服务热线
欧盟医疗器械注册必备参考网站
欧盟法律官网
欧盟法律官方网站
网址:https://eur-lex.europa.eu/homepage.html
集中展示了欧盟的各种法律文件,如条例(Regulations)、指令(Directives)、决定(Decisions)、建议(Recommendations)和意见(Opinions)等。在医疗器械领域,像医疗器械法规(MDR)和体外诊断医疗器械法规(IVDR)等关键法规都能在此查询。这些法律文件涵盖了欧盟活动的广泛领域,包括但不限于经济、贸易、环境、农业、社会政策、卫生健康、消费者保护等诸多方面,为用户提供了一站式的欧盟法律查询服务。
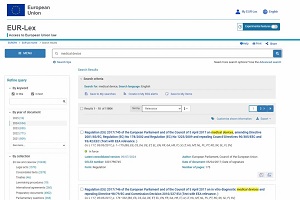
在主界面使用搜索引擎,输入关键词,例如 “medical device”,即可查阅相应医疗器械法规文件。
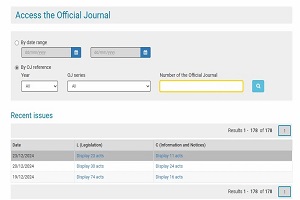
欧盟 Official Journal(欧盟官方公报)
网址:https://eur-lex.europa.eu/oj/direct-access.html
欧盟官方公报是欧盟法律行为、其他行为以及来自欧盟机构、团体、办公室和机构的官方信息的官方出版物,每天(周一至周五)以欧盟当时的24种官方语言发布,在紧急情况下也会在周六、周日和公共假日发布。可通过搜索功能,按照日期范围或特定的参考信息来查找所需的欧盟官方公报内容。公报目前包括两个系列:
-
L 系列(立法):主要包含欧盟的二级立法(主要是法规、指令、决定、意见和建议)以及国际协议,医疗器械相关的法规、指令等重要立法文件会在此发布,如 MDR 和 IVDR 的相关修订和补充信息,这些文件直接影响着医疗器械在欧盟市场的准入和运营,是医疗器械注册过程中必须遵循的重要准则。
-
C 系列(信息和通知):包含筹备行为、公告、欧盟法院判决摘要、欧洲审计法院年度报告、欧洲经济和社会委员会以及欧洲地区委员会的声明、欧盟计划和项目的兴趣表达呼吁等,为医疗器械企业提供了更广泛的行业信息和政策动态,有助于企业提前规划注册策略和产品布局。
欧盟委员会官网
欧盟委员会(Public Health)
网址:https://health.ec.europa.eu/index_en
欧盟委员会的 Public Health(公共卫生)部门在保障欧盟公民健康方面发挥着关键作用。致力于制定和实施一系列公共卫生政策与战略,涵盖传染病防控、慢性病管理、医疗保健体系优化、药品监管、健康促进等多个领域。在医疗器械方面,提供了医疗器械指令与法规、分类、EUDAMED 数据库、指导文件、专家小组、主题资讯、最新动态及相关法规链接等多方面信息,涵盖医疗器械监管全流程及关键要点。例如,其发布的医疗器械分类规则指导企业准确界定产品类别,从而按照相应的注册程序进行申报;指导文件则为企业准备注册资料提供了详细的规范和要求,帮助企业顺利完成医疗器械的注册流程,确保产品符合欧盟的安全和质量标准,保障公众健康。
欧盟医疗器械和体外诊断医疗器械法规下的协调标准相关内容。
网址:https://health.ec.europa.eu/medical-devices-topics-interest/harmonised-standards_en
网站主要涉及欧盟医疗器械和体外诊断医疗器械法规下的协调标准相关内容。这些协调标准是由欧洲标准化组织(CEN 和 CENELEC)根据欧盟委员会依据相关法规发布的标准化请求制定的,自愿使用这些标准可被推定为符合法规要求。在医疗器械注册中,企业参照这些协调标准来设计、生产和测试产品,能够证明产品符合欧盟法规对于安全性和有效性的基本要求,有助于提高注册的成功率和效率,同时也保障了产品在欧盟市场上的质量和性能一致性。

欧盟医疗器械协调小组(Medical Device Coordination Group)MDCG指南
网址:https://health.ec.europa.eu/medical-devices-sector/new-regulations/guidance-mdcg-endorsed-documents-and-other-guidance_en
MDCG 指南为医疗器械制造商、公告机构、其他相关方等提供了在遵循欧盟医疗器械法规时的具体指导和参考,有助于确保医疗器械的安全性、有效性和合规性。在医疗器械注册环节,MDCG 指南详细说明了注册所需的临床数据要求、技术文件编制规范、风险评估方法等关键内容,例如 MDCG 发布的关于临床评估的指南,指导企业如何收集、分析和呈现临床数据以支持注册申请,使企业能够更准确地把握注册要点,避免因资料不完整或不符合要求而导致的注册延误或失败,有力地推动了医疗器械的注册进程。

公告机构相关网站
公告机构Nando网站
网址:https://ec.europa.eu/growth/tools-databases/nando/
公告机构 nando 网站是欧盟委员会的官方网站,用于查询欧盟范围内所有被授权进行医疗器械符合性评估的公告机构的信息。在医疗器械注册过程中,企业需要选择合适的公告机构对其产品进行符合性评估,以获得 CE 认证等相关认证,从而进入欧盟市场。该网站提供的公告机构列表及其详细信息,包括授权范围、审核能力、联系方式等,帮助企业筛选出符合自身产品类别和技术要求的公告机构,确保产品能够得到专业、准确的评估,顺利完成注册手续,开启欧盟市场的大门。
欧洲医疗器械公告机构协会的官方网站team-nb
网址:https://www.team-nb.org
会发布与医疗器械行业相关的最新消息,如法规更新、政策变化、协会活动等,帮助会员和其他关注者及时了解行业动态.

其它公告机构网址
3EC International a.s.(Notified Body No. 2265)
https://www.3ec.sk/en/services/product-certification-mdr/
BSl Group The Netherlands B.V.(Notified Body number:2797)
https://www.bsigroup.com/en-MY/medical-devices/our-services/ce-marking/
欧洲数据库
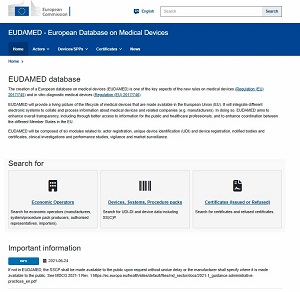
EUDAMED
网址:https://ec.europa.eu/tools/eudamed/#/screen/home
EUDAMED 是欧盟医疗器械法规(MDR)和体外诊断医疗器械法规(IVDR)框架下建立的一个全面的集中式数字平台,旨在存储和维护欧盟市场上流通的医疗器械的关键信息,是欧盟医疗器械监管领域的核心部分。在医疗器械注册阶段,制造商需要在 EUDAMED 上注册设备信息,包括产品的技术文件、UDI(唯一设备标识)等详细资料,这些信息将用于监管机构对产品的审核和监管,确保产品的安全性和可追溯性。同时,EUDAMED 中的证书和公告机构模块记录了公告机构颁发的证书信息,方便监管机构和企业查询和验证,为医疗器械的注册和市场准入提供了有力的支持和保障,有效维护了欧盟医疗器械市场的秩序和公众健康。