服务热线
印度尼西亚医疗器械及体外诊断产品的分类指南(一)
1999 年第 8 号《消费者保护法》(1999 年印度尼西亚共和国公报第 42 号,印度尼西亚共和国公报增刊第 3821 号);
2009 年第 36 号《卫生法》(2009 年印度尼西亚共和国公报第 144 号,印度尼西亚共和国公报增刊第 5063 号);
1998 年第 72 号《药品和医疗器械政府条例》(1998 年印度尼西亚共和国公报第 138 号,印度尼西亚共和国公报增刊第 3781 号);
2013 年卫生部第 76 号《医疗器械和家用健康产品广告条例》(2014 年印度尼西亚共和国公报第 192 号);
2014 年卫生部第 70 号《家用卫生设备和家用健康产品公司条例》(2014 年印度尼西亚共和国公报第 1563 号);
2015 年第 35 号总统条例《关于卫生部》;
2015 年印度尼西亚共和国卫生部第 64 号条例《关于卫生部的组织和治理工作》;
2010 年卫生部第 1189 号条例《关于医疗器械生产证书和家庭健康产品》。
医疗设备
医疗设备系指用于人体的仪器、装置、机器、工具 和(或) 植入物,体外试剂和校准器、软件、材料(单独或组合使用的材料),具备以下一项或多项功能目的:
1.用于疾病的诊断、预防、监测、治疗或缓解;
2.针对损伤进行诊断、监测、治疗、缓解或促进恢复;
3.实施检查、替换、修改或提供解剖学支持或生理过程辅助;
4.实现对生命的支持或维持;
5.用于控制受精过程;
6.承担医疗设备的消毒功能;
7.通过体外检测人体标本以提供医学或诊断信息,其主要作用于人体内部或表面,虽不直接涉及药理学、免疫学和代谢过程,但在达成其功能时可借助这些过程。
体外诊断(DIV)产品
体外诊断产品是指任何试剂、试剂产品、校准器、对照材料、试剂盒、仪器、设备或系统,可单独或与其他试剂、产品、校准器、对照材料、试剂盒、仪器、设备或系统联合运用,产品所有者预期其在体外用于检查任何标本,涵盖血液或源自人体的供体组织,主要旨在提供如下信息:
1.有关生理或病理状况或异常状态的信息;
2.确定任何血液或组织供体与潜在接受者之间的安全性和适用性等相关信息;
3.用于监测治疗措施的信息;包括标本容器。
有源医疗设备
有源医疗设备是指依靠电能或其他非人体直接产生的能量源(如重力)来实现操作,并通过改变该能量以达成工作效能的医疗设备。旨在实现能量、物质或其他元素在有源医疗设备与患者之间转移的医疗设备,若未改变其性质,则不纳入有源医疗设备范畴。注:独立的软件目前属于医疗设备的定义范畴,被视作有源医疗设备。
主动治疗医疗设备
单独使用或与其他医疗设备协同使用的有源医疗设备,其用途在于支持、修改、替代或改善生物功能或结构,以实现治疗疾病、减轻伤害或残疾的目标。
有源诊断医疗设备
单独使用或与其他医疗设备相结合使用的有源医疗设备,主要用于提供检测、诊断、监测或辅助治疗生理状况、健康水平、疾病或出生缺陷的信息。
无源医疗设备
使用除有源医疗设备所采用能源之外的其他能源进行操作的医疗设备。
侵入式医疗设备
穿透身体整体或部分的医疗设备,其进入途径包括身体自然孔口或身体表面。
非侵入式医疗设备
不直接穿透整个或部分身体的医疗设备,其与身体的接触方式不涉及通过身体自然孔口或身体表面进行穿透。
使用期限
1.短期:连续使用医疗设备少于 60 分钟;
2.中期:连续使用医疗设备在 60 分钟至 30 天之间;
3.长期:连续使用医疗设备超过 30 天。
医疗设备依据其在使用过程中所构成的风险进行分类。基于这些风险考量,健康设备被细致划分为以下四个类别:
| 分类 | 风险级别 | 示例 |
| A | 低风险 | 胶片观察器、外科器械、手术手套、氧气面罩 |
| B | 低-中等风险 | 血压袖带、蒸汽灭菌器 |
| C | 中-高风险 | 病人监护仪、X光机 |
| D | 高风险 | 心脏支架、起搏器 |
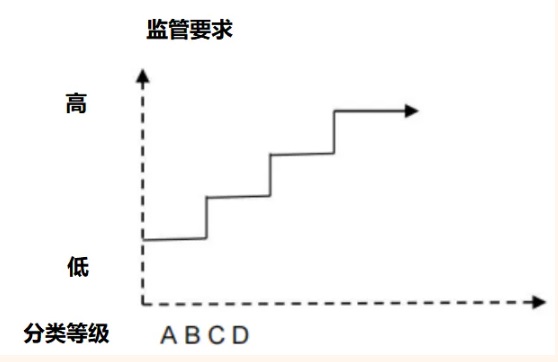
医疗设备风险类别与注册要求的关系示意图
图中清晰显示从低到高风险类别 A、B、C、D,注册要求在文件审核深度、临床试验规模与严格程度、质量体系认证标准等方面逐渐提高。
若一个医疗设备符合两个或更多医疗设备类别的判定规则,那么该设备的类别将严格依据最高风险类别予以确定。这一原则旨在确保对高风险特性的设备实施最为严格的监管措施,以充分保障公众健康和安全。
若一个医疗设备设计用于与其他医疗设备组合使用,则每个此类医疗设备应分别进行独立分类。这是因为组合使用可能改变单个设备的风险特征,分别分类有助于准确评估和管理整体风险。
医疗设备的分类受以下多方面因素影响:
1.工具与身体接触的时间长度:
接触时间长短与风险程度紧密相关。较长时间的接触为不良事件的发生提供了更多机会,例如长期植入体内的设备,如心脏起搏器,相较于短期接触皮肤表面的设备,如一次性电极片,其风险显著更高。长期接触可能引发多种潜在问题,包括感染风险增加、组织长期受压或磨损导致的损伤、生物相容性问题随时间推移而加剧等。这些潜在风险的增加使得在分类时需将长期接触设备归为较高风险类别,以确保对其进行更为严格的监管和评估。
2.进入身体的深度和位置:
设备进入人体的深度和作用位置对风险评估至关重要。侵入人体内部越深、越接近重要器官的设备,一旦发生故障或不良反应,其后果往往更为严重。例如,神经外科手术中使用的深部脑刺激器,其操作部位位于大脑深部,与仅在体表使用的温度计相比,风险不可同日而语。前者若出现故障可能直接影响神经功能,导致严重的神经系统并发症,甚至危及生命;而后者的风险主要局限于局部皮肤反应等较轻程度。因此,在分类时,侵入深度和位置是关键考量因素,深部侵入且靠近重要器官的设备通常被认定为高风险类别,需满足更严格的法规要求。
3.医疗设备的组合情况:
复杂的设备组合可能引发协同作用或相互干扰,从而增加风险的不确定性。不同设备组合使用时,可能出现诸如电磁兼容性问题、物理连接稳定性问题、药物-器械相互作用等新的风险因素。例如,在心脏介入手术中,血管造影机与心脏起搏器同时使用,若两者电磁兼容性不佳,可能导致起搏器功能异常,进而影响心脏正常节律。因此,对于组合使用的医疗设备,在分类时需综合评估组合后的整体风险,确保各个设备在协同工作时的安全性和有效性,避免因组合使用而带来的潜在风险被忽视。
4.作为诊断工具或维护用途的预期用途:
诊断工具的准确性直接关系到后续治疗决策,若诊断失误,可能导致患者接受不恰当的治疗,从而延误病情或引发其他严重后果。例如,病理诊断设备若出现误诊,可能使患者接受不必要的手术或错过最佳治疗时机。而维护生命支持类设备,如呼吸机,其主要功能是在患者生命垂危时维持生命体征,若该类设备失效,将直接危及患者生命。这些不同的预定用途决定了其各自独特的风险特征,在分类过程中需充分考虑其对患者健康的潜在影响程度,以确保分类的准确性和合理性。
5.局部到全身的影响:
部分医疗设备虽初始作用于局部,但可能引发全身性影响。例如,局部皮肤感染若未得到有效控制,可能通过血液循环扩散至全身,引发全身性炎症反应综合症,严重威胁患者生命健康。这种潜在的全身性影响极大地提升了设备的风险级别,因此在分类时,必须全面评估设备对整体生理机能的潜在影响范围,不仅仅局限于局部作用部位,还需考虑其可能引发的全身连锁反应,以准确判断其风险类别,实施相应的监管措施。
6.在体内的作用机制:
不同的作用机制决定了医疗设备的风险特性。某些设备主要通过物理作用实现功能,如骨折固定用的钢板和螺钉,其风险主要集中于物理结构的稳定性和生物相容性方面;而另一些设备涉及化学或生物作用机制,如药物洗脱支架,其在释放药物过程中需精确控制药物剂量、释放速率等因素,以避免药物过量或不足引发的不良后果。相比单纯物理支撑类设备,涉及复杂化学或生物作用机制的设备风险评估更为复杂,在分类时需依据其独特的作用机制进行更为细致的风险分析,确保分类结果与实际风险相符。
7.对身体的生物效应(如适用):
产生生物效应的设备可能改变人体生理状态,若效应不可控或引发不良后果,风险较高。例如,电刺激神经类设备,其通过施加电脉冲刺激神经以达到治疗目的,但如果电脉冲参数设置不当,可能过度刺激神经组织,导致神经损伤等不可逆后果。因此,在分类时需深入评估此类设备对身体的生物效应,包括效应的类型、强度、持续时间以及潜在的长期影响等,以确定其风险类别,保障患者安全使用。
8.接触破损皮肤(如适用):
破损皮肤破坏了人体的天然屏障功能,为微生物侵入人体提供了便捷途径。接触破损皮肤的设备,如伤口敷料、皮肤缝合器等,增加了感染风险,且感染可能进一步扩散引发全身性感染。所以,此类设备在分类时应充分考虑这一特殊因素对风险的提升作用,相较于不接触破损皮肤的设备,通常需满足更高的无菌标准和生物相容性要求,以降低感染风险,确保患者安全。
9、工具是否可重复使用:
可重复使用的医疗设备若清洁、消毒或灭菌不彻底,容易在不同使用者间传播病原体,引发交叉感染。例如,腹腔镜手术器械在多次使用过程中,若清洗和灭菌环节存在漏洞,残留的病原体可能感染后续使用者,导致严重的医源性感染事件。因此,设备的可重复使用性是分类时的重要考量点,对于可重复使用设备,需建立严格的清洗、消毒、灭菌规范和质量控制体系,并在分类过程中评估其重复使用相关风险,确保其安全性和有效性。
DIV 产品的风险分类受个人风险因素和对公共健康的风险影响。基于这些风险考量,DIV 产品分为以下四个类别:
| 分类 | 风险 | 示例 |
| A | 个人风险低(低个人风险),对公共健康的风险低(低公共健康风险) | 临床化学测试设备(临床化学分析仪、胆固醇检测设备、尿酸检测设备 |
| B | 个人风险中等(中等个人风险),对公共健康的风险低(低公共健康风险) | 自用妊娠检测试剂盒(自我妊娠检测) |
| C | 个人风险高(高个人风险),对公共健康的风险中等(中等公共健康风险) | 血糖测试设备、HLA测定设备、PSA筛查设备、风疹检测设备 |
| D | 个人风险高(高个人风险),对公共健康的风险高(高危公共健康风险) | 血液HIV筛查设备、HIV血液诊断设备 |
DIV 产品的类别对所需的注册要求产生显著影响。一般而言,DIV 产品的类别越高,注册要求所需的信息就越全面深入。
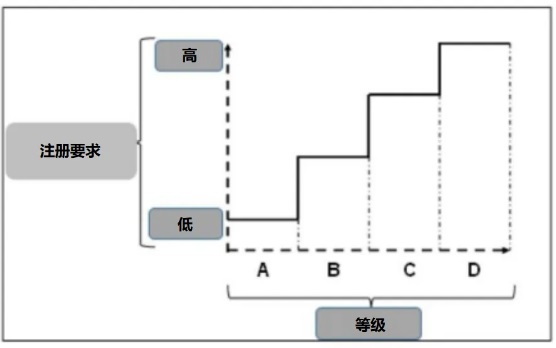
随着DIV产品风险类别增加的监管要求示意图

