服务热线
欧盟医疗器械CE认证
分类:法规注册咨询 发布人:admin 发布时间:2024-09-06 15:43 阅读:1653
自2021年5月起,欧盟医疗器械新法规2017/745(MDR法规)正式实施,意味着医疗器械应满足MDR法规并获得CE标志批准后,方可在欧洲经济区的31个国家/地区销售设备。
CE-MDR将医疗器械分为4个风险等级:
I类(低风险),如:手动轮椅、听诊器、绷带
IIa类(中低风险),如:正畸线、无创无呼吸、血氧仪、
IIb类(中高风险),如:人工晶状体、婴儿保温箱
III类(高风险),如:起搏器、人工心脏瓣膜、心血管缝合线
31个国家/地区分别是:
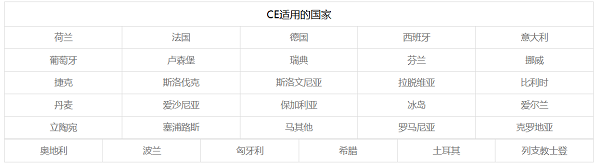
Notice:除美国、日本、澳大利亚等国,其它绝大多数国家认可CE认证转换的自由销售证书CFS/FSC。
医疗器械CE认证流程图:
.png)

